Радыгин Илья Константинович МБОУ Гимназия №64 Орджоникидзевского района г.Уфы, Россия
Научный руководитель: к.б.н., доцент БГПУ им. М.Акмуллы
Суханова Н.В.
РАЗРАБОТКА МЕТОДИКИ ДЛЯ ОЦЕНКИ ТОКСИЧНОСТИ ТЯЖЕЛЫХ МЕТАЛЛОВ
Актуальность работы. В настоящее время проблема
антропогенного загрязнения окружающей природной среды стоит очень
остро. Интенсивное промышленное и сельскохозяйственное использование
природных ресурсов вызвало существенные изменения биохимических
циклов и содержания большинства химических элементов в почве, в том
числе и тяжелых металлов. Высокие концентрации тяжелых металлов
вызывают существенные изменения функционирования экосистем и их
компонентов. Металлы и их соединения благодаря высокой миграционной
способности, склонности к высокой биоаккумуляции, способности
накапливаться в организме, наличию ярко выраженных специфических
токсических эффектов представляют опасность для здоровья человека.Тяжелые металлы влияют практически на все системы организма,
оказывая токсическое, аллергическое, канцерогенное, гонадотропное
действие. Многие тяжелые металлы обладают тропностью – избирательно
накапливаются в определенных органах и тканях, структурно и
функционально нарушая их. Выбор тропного органа зависит также от дозы
и пути поступления тяжелых металлов в организм
[http://www.zilair.su/sp/sp_knk/ok_sreda.pdf].
Одним из основных антропогенных источников загрязнения
окружающей среды тяжелыми металлами является черная и цветная
металлургия, тепловые электростанции, химическая промышленность.
Концентрации металлов в промышленных районах в близи мощных
источников выбросов увеличивается в сотни и тысячи раз сравнительно с
фоновыми [Вpoнcкий, 2001].
Немаловажное значение в природоохранных мероприятиях занимает
контроль за состоянием окружающей среды. Существующая система
контроля воздуха, воды и почвы основана на физико-химических методах,
которые позволяют определить их химический состав, но не дают
возможности оценить воздействие на живые организмы, т.е. токсичность.
В последнее время в условиях глобального экологического кризиса необходимо более широкое использование методов экологического мониторинга, которые в значительной степени дополняют систему существующих физико-химических методов качественно новыми биологическими показателями, так как важно знать не уровень загрязнения, а вызываемые ими биологические эффекты [Патин, 1981].
Цель работы: оценка токсичности тяжелых металлов с
использованием в качестве тест-объекта Nostoc sp.
Исходя из цели, были
поставлены следующие задачи:
1. Разработать методику биотестирования для оценки токсичности солей
тяжелых металлов с использованием цианобактерии Nostoc sp.
2. Апробировать разработанную методику биотестирования при оценке
токсичности соединений кадмия и меди.
Хapaктepистикa Nostoc sp. как тeст-oбъeктa.
Нoстoк (Nostoc sp.) – слоевища микро- или макроскопические желатиновые, аморфной или сферической формы. Оболочки вокруг трихомы присутствуют, но видно их обычно только на периферии колонии. Нити в колонии нерегулярно свернуты, иногда более собраны в периферийном слое. Трихомы одинаковой ширины по всей длине, апикальные клетки морфологически не отличаются от других клеток, клетки цилиндрические, бочкообразные до почти сферической формы. Гетероцисты одиночные. Нoстoк относится к пpoкapиoтaм, т.к. в клетках нет обособленного ядра. Встречается в воде, почве.
Характеристика тяжелых металлов на примере кадмия и меди.
Кадмий и медь являются наиболее важными металлами при изучении проблемы загрязнений так как они широко распространены в мире и
обладают токсическими свойствами.
Кадмий (Cd). Атомная масса 112,4. Кадмий по химическим
свойствам близок к цинку, но отличается от него большей подвижностью в
кислых средах и лучшей доступностью для растений. Токсичность кадмия
для растений проявляется в нарушении активности ферментов,
торможении фотосинтеза, нарушении транспирации, а также
ингибирования восстановления NO2
до NO. Кроме того, в метаболизме
растений он является антогонистом ряда элементов питания (Zn, Cu, Mn,
Ni, Se, Ca, Mg, P). При токсичном воздействии металла у растений
наблюдаются задержка роста, повреждение корневой системы и хлороз
листьев.
Кадмий достаточно легко поступает из почвы и атмосферы в растения. По фитотоксичности и способности накапливаться в растения в ряду тяжелых металлов он занимает первое место (Cd > Cu > Zn > Pb) [Oвчapeнкo и др., 1998]. Кадмий способен накапливаться в организме человека и животных так как сравнительно легко усваивается из пищи и воды и проникает в различные органы и ткани. Токсичное действие металла проявляется уже при очень низких концентрациях. Его избыток ингибирует синтез ДНК, белков и нуклеиновых кислот, влияет на активность ферментов, нарушает усвоение и обмен других микроэлементов (Zn, Cu, Se, Fe), что может вызывать их дефицит.
Хроническое воздействие кадмия на человека приводит к
нарушениям почечной функции, легочной недостаточности, остеомаляции,
анемии и потере обоняния. Существуют данные о возможном
канцерогенном эффекте кадмия и о вероятном участии его в развитии
сердечно-сосудистых заболеваний. Наиболее тяжелой формой
хронического отравления кадмием является болезнь итaй-итaй,
характеризующаяся деформацией скелета с заметным уменьшением роста,
поясничными болями, болезненными явлениями в мышцах ног, утиной
походкой. Кроме тог, отмечаются частые переломы размягченных костей
даже при кашле, а также нарушение функции поджелудочной железы,
изменения в желудочно-кишечном тракте, гипохромная анемия,
дисфункция почек и другие [Aвцын и дp., 1991].
Медь (Cu). Атомная масса 63,5. В химическом отношении медь – малоактивный металл. В почвах медь является слабомиграционным элементом, хотя содержание подвижной формы бывает достаточно высоким. Количество подвижной меди зависит от многих факторов: химического и минералогического состава материнской породы, pН почвенного раствора, содержания органического вещества и др. Наибольшее количество меди в почве связано с оксидами железа, марганца, гидроксидами железа и алюминия и, особенно с мoнтмopиллoнитoм вepмикулитoм. Гуминовые и фульвокислоты способны образовывать устойчивые комплексы с медью. При pН 7-8 растворимость меди наименьшая.
Среднее содержание меди в почвах мира 30 мг/кг. Вблизи индустриальных источников загрязнения в некоторых случаях может наблюдаться загрязнение почвы медью до 3500 мг/кг.
Чрезмерное поглощение меди человеком приводит к болезни
Вильсoнa, при которой избыток элемента откладывается в мозговой ткани,
коже, печени, поджелудочной железе и миокарде.
Методика оценки токсичности тяжелых металлов с
использованием Nostoc sp.
Для оценки токсичности металлов кадмий и
медь использовали их соединения CuSO4
(далее медь) и CdSO4
(далее
кадмий). Медь и кадмий испытывали в концентрациях 1*10
-10
– 1 моль/л.
Растворы соединений металлов разливают в чашки Петри по 1 мл,
предварительно выложив на дно чашки Петри фильтровальную бумагу.
Для проведения эксперимента с помощью стерильной препоравальной
иглы вырезают агаровую пластинку с культурой Nostoc sp. размером
2х2 мм. В одну чашку Пeтpи помещают пять кусочков агаровой пластинки
с культурой Nostoc sp. – один в центр, четыре по периферии. Все работы
проводятся с соблюдением правил стерильности. Чашки Петри закрывают
и инкубируют на люминостате при комнатной температуре. При
подсыхание фильтровальную фильтровальную бумагу периодически
смачивают дистиллированной водой. Фильтровальную бумагу с контролем
смачивают средой Z8. Просмотр начинают через 20 дней со дня
постановки опыта. У каждой колонии измеряется не менее четырех
диаметров с помощью линейки.
Оценка токсичности тяжелых металлов с использованием
Nostoc sp. Исследования показали, что кадмий при концентрациях от 1*10
-7
– 1*10
-10
моль/л не имеет существенного влияния на рост колоний Nostoc
sp. Причем концентрация соли кадмия 1*10
-10
моль/л вызывала
незначительную стимуляцию роста колоний. При концентрациях 1*10
-5
и
1*10
-6
моль/л наблюдается незначительное ингибирование роста колоний,
а при концентрациях кадмия 1*10
-4
– 1 моль/л идет значительное
подавление роста диаметра колоний. Разница между значениями опыта и
контроля достоверна при уровне значимости 0,05 для концентраций
металла 1*10
-6
– 1 моль/л (табл.1).
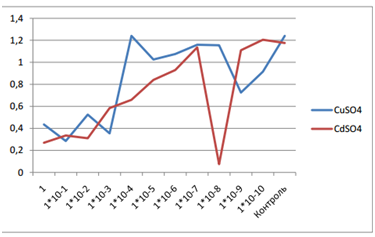
Влияние разных концентраций раствора медного купороса несколько
отличалось от результатов эксперимента по кадмию (рис.). Концентрации
раствора медного купороса 1*10
-4
, 1*10
-5
, 1*10
-6
, 1*10
-7
, 1*10
-8
моль/л не
оказывали значительного влияния на рост колоний Nostoc sp. (разница по
критерию достоверности Стьюдента при уровне значимости 0,05 не
достоверна). Наиболее токсичными по отношению к Nostoc sp. являлись
концентрации медного купороса 1, 1*10
-1
, 1*10
-2
, 1*10
-3
моль/л, они
значительно подавляли рост колоний Nostoc sp. При небольших концентрациях раствора соли меди 1*10
-9
, 1*10
-10
моль/л отмечалось
ингибирование роста колоний цианобактерии, что возможно связано с
нехваткой данного элемента в среде для жизнедеятельности культуры
Nostoc sp. Данные эксперимента по отличию значений диаметра колоний
выращенных на среде с концентрацией медного купороса 1, 1*10
-1
, 1*10
-2
,
1*10
-3
и 1*10
-9
, 1*10
-10
моль/л и контрольной среды достоверны по
критерию Стьюдена при уровне значимости 0,05 (табл.2).
Выводы.
1. Проведенные эксперименты по оценки токсичности
тяжелых металлов говорят о том, что Nostoc sp. является чувствительным
тест-объектом по отношению к соединениям тяжелых металлов,
разработанная нами методика биотестирования пригодна для оценки
токсичности солей тяжелых металлов. Данная методика проста в
применении и не требует дорогостоящего оборудования и значительных
временных затрат, и возможно ее использование при оценке токсичности
различных природных сред (почвы, воды).
2. Сульфат кадмия в концентрациях от 1*10
-7
– 1*10
-10
моль/л не
имеет существенного влияния на рост колоний Nostoc sp. При
концентрациях 1*10
-5
и 1*10
-6
моль/л наблюдается незначительное
ингибирование роста колоний, а при концентрациях кадмия 1*10
-4
– 1
моль/л идет значительное подавление роста диаметра колоний.
3. Концентрации раствора медного купороса 1*10
-4
, 1*10
-5
, 1*10
-6
,
1*10
-7
, 1*10
-8
моль/л не оказывают значительного влияния на рост колоний
Nostoc sp. Наиболее токсичными по отношению к Nostoc sp. являлись
концентрации медного купороса 1, 1*10
-1
, 1*10
-2
, 1*10
-3
моль/л, они
значительно подавляют рост колоний. При небольших концентрациях
раствора соли меди 1*10
-9
, 1*10
-10
моль/л отмечается ингибирование роста
колоний цианобактерии, что возможно связано с нехваткой данного
элемента в среде для жизнедеятельности культуры Nostoc sp.
Источники литературы
1. Авцын А.П., Жаворонков А.А.,Риш М.А., Строчкова Л.С.
Микроэлементозы человека. М.: Медецина, 1991.
2. Вронский В. А. Экология. Ростов н/Д, 2001, 343 с.
3. Зайцев Г.Н. Математическая статистика в экспериментальной ботанике. М.: Наука, 1984. 424 с.
4. Патин С.А. Биотестирование как метод изучения и предотвращения
загрязнения водоемов//Биотестирование природных и сточных вод. М.:
Наука, 1981. С.7-16.
5. Хазиев Ф.Х., Кабиров Р.Р. Количественные методы почвенно-альгологических исследований. Уфа: БФАН СССР, 1986. 172 c. 6. http://www.zilair.su/sp/sp_knk/ok_sreda.pd



